http://www.ras.ru/news/shownews.aspx?id=218a1acd-ebe2-45e3-901e-0e322422d88d&print=1
© 2024 Российская академия наук
Сотрудники Института теоретической и экспериментальной биофизики РАН (Пущино) и Саратовского национального исследовательского государственного университета им. Н.Г. Чернышевского синтезировали наночастицы на основе оксида церия и биоактивной молекулы пирролохинолинхинона, которые при действии рентгеновских лучей избирательно защищают здоровые клетки от гибели.
Наночастицы поддерживают работу антиоксидантных систем нормальных клеток, при этом у раковых клеток, напротив, стимулируют выработку активных форм кислорода, которые приводят к повреждению клеточных структур. Такой эффект, по всей видимости, связан с тем, что раковые клетки имеют кислотность, отличную от нормальных клеток. Благодаря этому разработка может быть использована, чтобы уменьшить негативное воздействие лучевой терапии при лечении онкологических заболеваний. Результаты исследования, поддержанного грантом Российского научного фонда (РНФ), опубликованы в журнале Antioxidants.
Один из наиболее распространённых методов лечения рака — лучевая терапия, при которой опухоль уничтожают с помощью рентгеновского, гамма- или другого ионизирующего излучения. Оно запускает окислительные процессы, которые повреждают ДНК, белки, мембраны и прочие структуры, в результате чего клетки гибнут. При этом лучевая терапия действует неизбирательно — наравне с опухолевыми погибают и здоровые клетки, что плохо сказывается на состоянии организма. Поэтому учёные ищут способы сделать так, чтобы лучевая терапия запускала окисление только в раковых клетках.
Авторы работы синтезировали наночастицы на основе оксида церия — биосовместимого соединения, способного вступать в большое количество окислительно-восстановительных реакций. Оксид церия может защищать здоровые клетки от повреждений во время лучевой терапии, при этом усиливая повреждения ДНК в раковых клетках. Авторы решили повысить избирательность оксида церия, присоединив к нему пирролохинолинхинон — биоактивную молекулу, которая обладает высоким антиоксидантным эффектом и участвует в регуляции работы митохондрий.
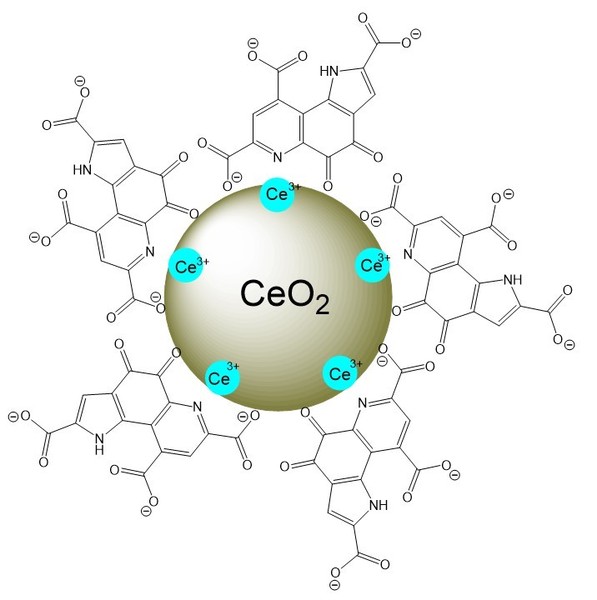
Схематическое изображение наночастиц церия, модифицированных пирролохинолинхиноном
Авторы осадили наночастицы из раствора хлорида церия и химически «навесили» на их поверхность молекулы пирролохинолинхинона. Исследователи в разных концентрациях нанесли полученные комплексы на здоровые клетки соединительной ткани мыши — фибробласты, — а также на раковые клетки. Это позволило определить количества, в которых наночастицы не вызывают массовой гибели ни одного из типов клеток. В дальнейшем в экспериментах с рентгеновским излучением исследователи использовали именно эти концентрации наночастиц.
Оказалось, что рентгеновские лучи снижают жизнеспособность фибробластов на 75 %, а раковых клеток — на 32 %. Однако после обработки наночастицами и облучения выживаемость здоровых фибробластов увеличилась на 45 % по сравнению с контрольными клетками, которые не испытывали никаких воздействий, но тоже в небольшом количестве гибли из-за естественных причин. В случае опухолевых клеток выживаемость оказалась на 31—37 % ниже, чем в контрольной группе — это сопоставимо с результатами, полученными при одном лишь облучении без использования наночастиц. Таким образом, наночастицы практически не снижают выживаемость нормальных клеток, но значительно понижают её у раковых.

Микрофотография наночастиц
Авторы комментируют: избирательное токсичное действие в отношении раковых клеток объясняется тем, что в раковых клетках кислотность среды отличается от таковой у здоровых. Из-за этого изменяются свойства наночастиц, и под действием рентгеновских лучей они не оказывают такого же антиоксидантного эффекта.
«Наблюдаемый эффект связан с тем, что наночастицы оксида церия, модифицированные пирролохинолинхиноном, снижают уровень активных форм кислорода в фибробластах и тем самым спасают их от окисления. Благодаря этому их можно использовать, чтобы уберечь здоровые клетки от гибели при лучевой терапии рака. В дальнейшем мы планируем провести эксперименты на других типах здоровых и раковых клеток, чтобы лучше понять, как в каждом случае работают наночастицы», — рассказывает руководитель проекта, поддержанного грантом РНФ, ведущий научный сотрудник и заведующая лабораторией изотопных исследований ИТЭБ РАН кандидат биологических наук Нелли Попова.
Источник: РНФ.